En ocasiones, el medio ambiente sufre cambios que pueden ser debidos a actividades humanos, como incendios, industrias, utilización de vehículos, etc, y otras veces se deben a actividades naturales, por ejemplos, las erupciones volcánicas, tormentas u otros fenómenos meteorológicos.
La química analiza los cambios para tratar de determinar la causa, y si es posible, corregirla y buscar una solución.
Índice:
1. Incremento del efecto invernadero.
2. La lluvia ácida.
3. La destrucción de la capa de ozono.
4. Contaminación y purificación del aire.
5. Contaminación y purificación del agua.
4. Contaminación y purificación del aire.
5. Contaminación y purificación del agua.
6. Recuperación de basuras.
- Opinión personal.
- Bibliografía
- Opinión personal.
- Bibliografía
1. Incremento del efecto invernadero
- A la Tierra llega la radiación del Sol que le aporta luz y calor. Una parte de esa radiación es absorbida, pero otra es reflejada por la propia Tierra hacia la atmósfera, de este balance resulta que la Tierra tiene una determinada temperatura en la que se desarrolla la vida. Pero cuando la atmósfera tiene mucho dióxido de carbono, la radiación que refleja la Tierra es reflejada de nuevo por la capa de contaminantes y aumenta la temperatura del planeta.
- Los incendios y las combustiones fósiles (las que producen en los coches, calefacciones, fábricas, etc), provocan un aumento de la concentración de dióxido de carbono en la atmósfera.
- El aumento de la temperatura de la Tierra puede provocar graves daños, como el deshielo de los casquetes polares y el aumento del nivel de las aguas en la Antártida y Groenlandia. Para controlar este aumento, muchos países firmaron en 1997 un convenio, el PROTOCOLO DE KYOTO, por el cual se comprometían a controlar sus emisiones de gases contaminantes.
2. La lluvia ácida
El agua es una sustancia neutra, con pH 7 (potencial de Hidrógeno), por lo tanto, la lluvia debería ser neutra. Pero en determinadas zonas de la Tierra se producen combustiones que emiten a la atmósfera grandes cantidades como dióxido de carbono, monóxido de nitrógeno y dióxido de azufre.
En la atmósfera, los óxidos de nitrógeno y de azufre se combinan con más oxígeno, transformándose en compuestos que, si se mezclan con agua, se convierten en ácido nítrico y ácido sulfúrico. Cuando llueve, la lluvia que cae es ácida y causa graves daños a la vegetación, e incluso puede destruir bosques enteros.
Estas son las ecuaciones químicas de las reacciones de antes:
- Los incendios y las combustiones fósiles (las que producen en los coches, calefacciones, fábricas, etc), provocan un aumento de la concentración de dióxido de carbono en la atmósfera.
- El aumento de la temperatura de la Tierra puede provocar graves daños, como el deshielo de los casquetes polares y el aumento del nivel de las aguas en la Antártida y Groenlandia. Para controlar este aumento, muchos países firmaron en 1997 un convenio, el PROTOCOLO DE KYOTO, por el cual se comprometían a controlar sus emisiones de gases contaminantes.
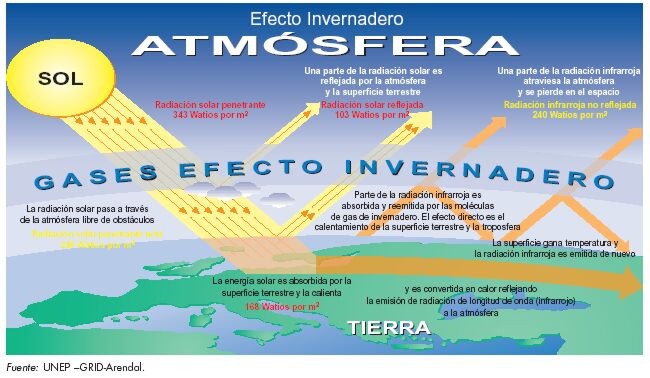 |
| Efecto invernadero. Derecho del autor: |
2. La lluvia ácida
El agua es una sustancia neutra, con pH 7 (potencial de Hidrógeno), por lo tanto, la lluvia debería ser neutra. Pero en determinadas zonas de la Tierra se producen combustiones que emiten a la atmósfera grandes cantidades como dióxido de carbono, monóxido de nitrógeno y dióxido de azufre.
En la atmósfera, los óxidos de nitrógeno y de azufre se combinan con más oxígeno, transformándose en compuestos que, si se mezclan con agua, se convierten en ácido nítrico y ácido sulfúrico. Cuando llueve, la lluvia que cae es ácida y causa graves daños a la vegetación, e incluso puede destruir bosques enteros.
Estas son las ecuaciones químicas de las reacciones de antes:
2 NO + 3/2 O2 ---------> N2O5 ; N2O5 + H2O ----------> HNO3 (Ácido nítrico)
SO2 + 1/2 O2 ----------> SO3 ; SO3 + H2O -----------> H2SO4 (Ácido sulfúrico)
 |
| Lluvia ácida. Derecho del autor: http://hangar1elblog.com.mx/?p=6856 |
3. La destrucción de la capa de ozono
Entre 15 y 40 km de altura sobre la superficie de la Tierra se extiende una capa denominada estratosfera que contiene ozono, un gas cuya molécula está formada por tres átomos de oxígeno.
El ozono tiene la propiedad de absorber una parte de la radiación ultravioleta procedente del Sol que es dañina para los seres vivos.
A partir de 1980, los investigadores comenzaron a darse cuenta de que había disminuido el grosor de la te hecho se capa de ozono sobre Antártida; es lo que se conoce como el "agujero de la capa de ozono". Es hecho se relacionó con la emisión a la atmósfera de ciertos gases, como los CFC (clorofluorocarbonos), gases que forman parte de muchos sprays y sistemas de refrigeración, como los que hay en los frigoríficos y en el aire acondicionado, que no se descomponen hasta que llegan a la estratosfera y destruyen el ozono.
El inconveniente es que los CFC son muy estables en la atmósfera, por lo que su efecto no desaparecerá de inmediato, aunque dejen de emitirse.
*Más información de los CFC: http://es.wikipedia.org/wiki/CFC
*Más información de los CFC: http://es.wikipedia.org/wiki/CFC
 |
| Destrucción de la capa de ozono por los CFC. Derecho del autor: |
TE INTERESA SABER...
Lanzamiento de un globo sonda para estudiar la capa de ozono.
Las normas recientes prohíben el uso de CFC en los sprays para evitar que el agujero de la capa de ozono crezca, ya que si sigue disminuyendo el grosor de esta capa, aumentarán las radiaciones ultravioleta nocivas que llegan a la Tierra, lo que puede provocar la aparición de cáncer de piel y otros problemas en muchas personas y en otros seres vivos. Desde 2006 se han observado signos de recuperación en la capa de ozono, aunque deberán pasar algunas décadas, según los expertos, hasta que la recuperación sea completa.
| Lanzamiento de un globo sonda para estudiar la capa de ozono. Derecho del autor: |
Este es vídeo en el que habla de los CFC y la capa de ozono, el ataque de los CFC a la capa de ozono. Enlace: https://www.youtube.com/watch?v=aV5eu1tr46w
4. Contaminación y purificación del aire
El aire es una mezcla de gases formada por nitrógeno (78%), oxígeno (21%) y una pequeña cantidad (1%) de otros gases, como el dióxido de carbono, vapor de agua, argón, helio, etc.
 |
| Componentes del aire. Derecho del autor: |
Contaminación:
Algunas actividades hacen que cambie la composición del aire. En ocasiones, son debidas a la evolución de la propia naturaleza, como las emisiones volcánicas. Pero otras veces, lo son por las actividades humanas. Así, las combustiones que se producen en los vehículos de motor (coches, aviones, barcos, etc.), en las calefacciones, o en muchas industrias, hacen que lleguen a la atmósfera gases que provocan efectos no deseados.
Medidas:
Para evitar estos problemas, se instalan filtros que capturan estos gases y los hacen reaccionar con otras sustancias, con lo que se evita que lleguen a la atmósfera. En las industrias en las que se queman combustibles y se liberan dióxido de azufre y dióxido de carbono se instalan filtros en la salida de gases. Esto hace que los gases se transformen en sustancias no volátiles, como sulfatos o carbonatos, que ya no pueden llegar a contaminar la atmósfera.
Ejemplo:
Los catalizadores de los coches hacen que los óxidos de nitrógeno se descompongan en nitrógeno y oxígeno, que al salir a la atmósfera ya no contaminan.
 |
| Estructura de un catalizador. Derecho del autor: |
5. Contaminación y purificación del agua
El agua interviene en muchas actividades humanas, agrícolas e industriales; cada una de estas actividades hace que lleguen al agua otras sustancias que pueden modificar sus propiedades.
Contaminación:
En ocasiones, el agua arrastra componentes sólidos, esto sucede en las explotaciones mineras o en la limpieza de granjas. Otras veces se le añaden sustancias que se disuelven y cambian su acidez, como detergente u otros productos extraños que alteran su capacidad para mantener la vida: insecticidas, abonos, aceites u otros productos industriales. También se vierten aguas a temperatura más alta (aguas de refrigeración) que hacen que disminuya la cantidad de oxígeno disuelto.
 |
| Contaminación del agua. Derecho del autor: |
Medidas:
Para evitar los problemas de todos estos vertidos, las aguas que resultan de estos usos no se arrojan directamente a los ríos, lagos o al mar, sino que se someten a un proceso de depuración y potabilización que depende de la contaminación que arrastren.
Procedimiento de la depuración:
1) Las aguas se depositan en unas balsas para que su temperatura se iguale a la del ambiente.
2) Los sólidos que arrastran se van al fondo, y los aceites, a la superficie.
3) Se añaden otras sustancias para corregir la acidez o capturar las sustancias extrañas que llevan disueltas, con el fin de que se conviertan en sólidos y se vayan al fondo.
4) Si se desea utilizar el agua para el consumo humano, hay que someterla a un proceso final de potabilización, que consiste en eliminar cualquier microorganismo que contenga, para ello, se suele añadir una cierta cantidad de cloro.
 |
| Procedimiento de una planta depuradora. Derecho del autor: |
6. Recuperación de basuras
Las actividades humanas generan gran cantidad de desechos que denominan basuras.
Algunos de estos desechos tienen una vida muy larga, como los plásticos. Otros contaminan el suelo y las aguas, como los metales pesados y el contenido de las pilas y baterías. Finalmente, otros se descomponen , produciendo malos olores y permitiendo el desarrollo de microorganismos.
Debemos modificar nuestras costumbres a fin de:
- Reducir la cantidad de basuras que producimos.
- Reutilizar los materiales para aprovechar al máximo su vida útil.
- Reciclar los materiales con el fin de obtener nuevos productos a partir de ellos.
Algunos consejos útiles:
- En tus compras, evita empaquetados innecesarios. Aprovecha las bolsas y reutilizarlas el mayor número de veces posible, y finalmente, deposítalas en el contenedor para su reciclaje.
- Si aprovechas las pilas y baterías hasta que se agoten, reducirás la cantidad que empleas. En la medida en que te sea posible, utiliza pilas recargables o baterías. Cuando se hayan agotado, échalas en el contenedor adecuado, en las plantas de tratamiento se extraerán los metales que contienen.
TE INTERESA SABER...
Una pila de mercurio puede contaminar hasta 600.000 L de agua (más de lo que consumen cuatro personas en toda su vida), y una pila alcalina, 175.000 L ; y una pila de botón, 12.000 L.
Las actividades humanas generan gran cantidad de desechos que denominan basuras.
Algunos de estos desechos tienen una vida muy larga, como los plásticos. Otros contaminan el suelo y las aguas, como los metales pesados y el contenido de las pilas y baterías. Finalmente, otros se descomponen , produciendo malos olores y permitiendo el desarrollo de microorganismos.
Debemos modificar nuestras costumbres a fin de:
- Reducir la cantidad de basuras que producimos.
- Reutilizar los materiales para aprovechar al máximo su vida útil.
- Reciclar los materiales con el fin de obtener nuevos productos a partir de ellos.
 |
| La regla de las tres erres. Derecho del autor: |
Algunos consejos útiles:
- En tus compras, evita empaquetados innecesarios. Aprovecha las bolsas y reutilizarlas el mayor número de veces posible, y finalmente, deposítalas en el contenedor para su reciclaje.
- Si aprovechas las pilas y baterías hasta que se agoten, reducirás la cantidad que empleas. En la medida en que te sea posible, utiliza pilas recargables o baterías. Cuando se hayan agotado, échalas en el contenedor adecuado, en las plantas de tratamiento se extraerán los metales que contienen.
 |
| La regla de las tres erres. Derecho del autor: |
TE INTERESA SABER...
Una pila de mercurio puede contaminar hasta 600.000 L de agua (más de lo que consumen cuatro personas en toda su vida), y una pila alcalina, 175.000 L ; y una pila de botón, 12.000 L.
 |
| ¡Hay que reciclar las pilas! Derecho del autor: |
- Opinión personal:
La química es una ciencia que estudia la composición, la estructura y las propiedades de la materia como los cambios que experimenta en las reacciones químicas y su relación de la energía. Evidentemente, la química está relacionada con el medio ambiente, ya que sufre cambios que son debidos a actividades humanos (utilización de vehículos, por ejemplo) y naturales (las erupciones volcánicas son una de ellas). Estos cambios pueden alterar el medio ambiente, y eso es malo.
1. Hablando del efecto invernadero, las industrias y los coches emiten el dióxido de carbono, y esto va a la atmósfera. Entonces, se concentra en la atmósfera y esto hacer aumentar la temperatura de la Tierra; y esto causa el deshielo de los casquetes polares y de Antártida. Para que esto no suceda, muchos países firmaron un convenio, el protocolo de Kyoto, por el cual se comprometían a controlar sus emisiones de gases contaminantes.
2. La lluvia ácida puede llegar a dañar bosques enteros y es peligroso para las personas y para los seres vivos. Esto también se debe a las emisiones de gases (dióxido de carbono, monóxido de nitrógeno y dióxido de azufre) de las industrias, por eso, tenemos que emitir menos estos gases contaminantes para proteger el medio ambiente y que no haya más lluvias ácidas.
3. En la estratosfera se encuentra un gas llamado ozono, y está formado por tres átomos de oxígeno. El ozono tiene la propiedad de absorber una parte de la radiación ultravioleta procedente del Sol que es dañina para los seres vivos. Y ahora descubre que la capa de ozono está disminuyendo el grosor, y en algún día del futuro, las radiaciones ultravioleta atraviesan la atmósfera y dañan a las personas (tener enfermedades de la piel, por ejemplo).
4. El aire contiene un gas muy importante para los seres vivos, el oxígeno, que nos sirve para respirar, sin él no hay vida, por eso es imprescindible. Y para esta fuente tan importante, no tenemos que contaminarla. Por eso tenemos que emitir menos gases contaminantes, y así, reducimos la contaminación del aire.
5. El agua también es una fuente imprescindible para la vida. Sin ella, tampoco viviríamos. Hay que contaminar menos y aprovechar más, ya que solo una pequeñísima parte de las aguas de la Tierra es útil para nosotros (agua dulce), y ahora, cada vez hay menos y llegará un día en el que se agotaría. Hay que tomar medidas serias para aprovecharla.
6. Las basuras las generamos todos los días, y debemos tirar a los cubos de basura correspondientes, así facilita su reciclaje. Y para contaminar más el medio ambiente, debemos producir menos basura y reutilizar las cosas, como las bolsas de compra, y reciclar los materiales, para obtener nuevos materiales a partir de ellos.
- Bibliografía:
- Libro de física y química de 3º ESO (Editorial: Santillana)
La química es una ciencia que estudia la composición, la estructura y las propiedades de la materia como los cambios que experimenta en las reacciones químicas y su relación de la energía. Evidentemente, la química está relacionada con el medio ambiente, ya que sufre cambios que son debidos a actividades humanos (utilización de vehículos, por ejemplo) y naturales (las erupciones volcánicas son una de ellas). Estos cambios pueden alterar el medio ambiente, y eso es malo.
1. Hablando del efecto invernadero, las industrias y los coches emiten el dióxido de carbono, y esto va a la atmósfera. Entonces, se concentra en la atmósfera y esto hacer aumentar la temperatura de la Tierra; y esto causa el deshielo de los casquetes polares y de Antártida. Para que esto no suceda, muchos países firmaron un convenio, el protocolo de Kyoto, por el cual se comprometían a controlar sus emisiones de gases contaminantes.
2. La lluvia ácida puede llegar a dañar bosques enteros y es peligroso para las personas y para los seres vivos. Esto también se debe a las emisiones de gases (dióxido de carbono, monóxido de nitrógeno y dióxido de azufre) de las industrias, por eso, tenemos que emitir menos estos gases contaminantes para proteger el medio ambiente y que no haya más lluvias ácidas.
3. En la estratosfera se encuentra un gas llamado ozono, y está formado por tres átomos de oxígeno. El ozono tiene la propiedad de absorber una parte de la radiación ultravioleta procedente del Sol que es dañina para los seres vivos. Y ahora descubre que la capa de ozono está disminuyendo el grosor, y en algún día del futuro, las radiaciones ultravioleta atraviesan la atmósfera y dañan a las personas (tener enfermedades de la piel, por ejemplo).
4. El aire contiene un gas muy importante para los seres vivos, el oxígeno, que nos sirve para respirar, sin él no hay vida, por eso es imprescindible. Y para esta fuente tan importante, no tenemos que contaminarla. Por eso tenemos que emitir menos gases contaminantes, y así, reducimos la contaminación del aire.
5. El agua también es una fuente imprescindible para la vida. Sin ella, tampoco viviríamos. Hay que contaminar menos y aprovechar más, ya que solo una pequeñísima parte de las aguas de la Tierra es útil para nosotros (agua dulce), y ahora, cada vez hay menos y llegará un día en el que se agotaría. Hay que tomar medidas serias para aprovecharla.
6. Las basuras las generamos todos los días, y debemos tirar a los cubos de basura correspondientes, así facilita su reciclaje. Y para contaminar más el medio ambiente, debemos producir menos basura y reutilizar las cosas, como las bolsas de compra, y reciclar los materiales, para obtener nuevos materiales a partir de ellos.
- Bibliografía:
- Libro de física y química de 3º ESO (Editorial: Santillana)
 |
| La química y el medio ambiente. Derecho del autor: |
















